RD-Biotech propose tout un panel de services sur mesure sur sa plateforme d’ingénierie des anticorps. En vous adressant à RD-Biotech, vous allez :

Une plate-forme intégrée pour le développement de vos anticorps thérapeutiques : de la cible au candidat
Bioproduction
RD-Biotech est une société de service reconnue pour son savoir-faire et son expérience dans le domaine des anticorps. La société dispose notamment d’une offre multi-technologique pour le développement d’anticorps à visée R&D, diagnostique, ou encore thérapeutique.
Production de vos candidats selon une stratégie adaptée et personnalisée en fonction de vos outils biologiques et des données disponibles :
- La cible (protéines, peptide, séquence protéique, données bibliographiques)
- Le clone sécréteur d’anticorps monoclonaux murins
- Les séquences nucléotidiques d’intérêt (séquences VH et VL)
- Les vecteurs d’expression prêts pour transfection
- La lignée cellulaire
En fonction du niveau d’avancement de votre projet, RD-Biotech a l’expertise et les plateformes technologiques pour :
- Exprimer votre cible (construction du vecteur et expression de l’antigène)
- Développer les anticorps monoclonaux (Hybridomes et phages display)
- Séquencer les anticorps monoclonaux
- Développer et produire vos anticorps recombinants
- Recombinants souris ou autres espèces, différents isotypes possibles
- Chimérisation de votre candidat
- Humanisation de votre candidat
- Modifications génétiques : Reformatage avec une autre espèce, changement d’isotypes, fragments d’anticorps (Fab, scFv, nanobodies), bispécifiques
- Système de production optimisé en cellules mammifères : cellules CHO, cellules HEK (autres cellules – nous consulter)
- Transfection à partir de vecteurs optimisés pour cellules mammifères
- Qualité R&D, « endofree » ou Grade High Quality
- Reproductibilité : procédure in vitro, milieu chimiquement défini, pour une excellente reproductibilité inter lots
- Pureté : système d’expression en cellules mammifères sérum free éliminant les risques de contamination par les composants sériques, et fournissant un niveau de pureté supérieur à 95 %
- Capacité : production de lots pilotes ou production large scale (jusqu’à plusieurs centaines de mgs)
- Rapidité : système d’expression à haut rendement permettant la fourniture des lots d’anticorps recombinants dans des délais très courts : Fourniture de lot de 100 mg d’anticorps recombinants purifiés et contrôlés en moins de 3 semaines.
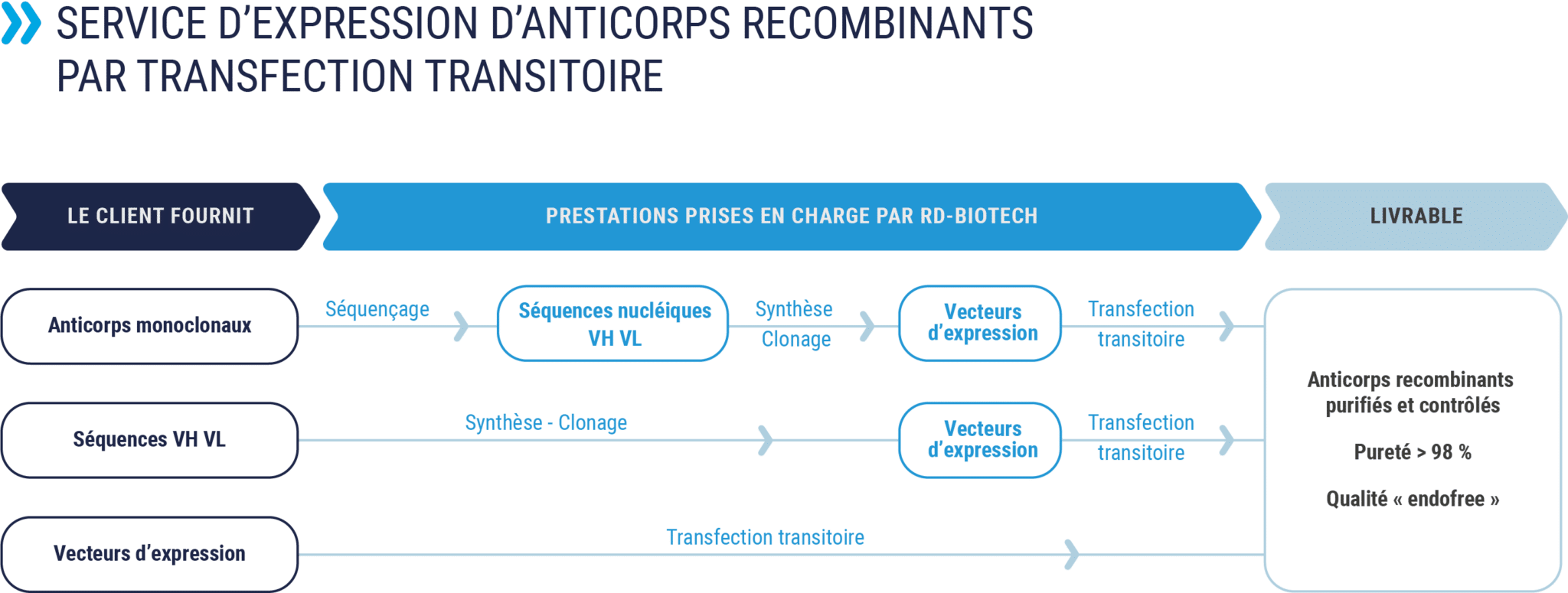
Production d’anticorps par transfection transitoire
Système CHO, HEK293 ou autres cellules
La procédure standard comprend les étapes suivantes (certaines étapes pouvant être prises en charge par le donneur d’ordre, à préciser).
- Étape Optionnelle : séquençage de l’anticorps monoclonal, chaînes lourdes et légère
- Étape 1 : synthèse des fragments variables VH et VL
- Étape 2 : sous clonage des fragments dans le vecteur d’expression. Contrôles qualité.
- Étape 3 : pilote d’expression des anticorps par transfection transitoire
- Étape 4 : suivi de production par ELISA (kit FastELISA)
- Étape 5 : purification du pilote par chromatographie d’affinité (Support protéine A)
- Étape 6 : contrôles qualité (services analytiques)
- Contrôle de pureté par électrophorèse en gel SDS-PAGE (conditions réductrices et non réductrices)
- Dosage des protéines totales par mesure d’absorbance (spectrophotomètre)
- Autres contrôles possibles, nous consulter
- Étape 7 : conditionnement et envoi du pilote, accompagné du rapport
Les délais de réalisation :
Étape 2 : 2 à 3 semaines
Étapes 3 à 5 : environ 3 semaines


Go No Go : Production et purification Large Scale selon la procédure validée (jusqu'au gramme)
En option, les anticorps produits in vitro peuvent être purifiés en conditions Endofree, ce qui nécessite l’usage de tampons et contenants apyrogènes.
Après l’étape de chromatographie d’affinité, la pureté de l’anticorps peut être améliorée par différentes méthodes :
- par une étape de SEC préparative qui permettra d’éliminer les agrégats ;
- par une étape de chromatographie d’échange d’ions, qui élimine également les endotoxines éventuellement présentes. Les anticorps monoclonaux produits in vitro par RD-Biotech en conditions Endofree ont un taux d’endotoxines inférieur à 1 EU/mg.
Des contrôles qualité supplémentaires peuvent être ajoutés aux contrôles de base, dépendant du cahier des charges du donneur et des applications.
- Test mycoplasme
- Test LAL permettant de déterminer le taux d’endotoxines bactériennes. Le test LAL (Limulus Amebocyte Lysate) est réalisé à l’aide d’un kit réglementaire selon le protocole du fournisseur.
- Test de non contamination bactérienne et fongique
- Contrôle par SEC analytique
- Dessalage des anticorps
- Contrôle de spécificité, d’activité biologique… (ELISA, Western Blotting, Octet, Cytométrie, bioessais à façon…)
- Dosage des résidus Protéine A (Kit RD-Biotech FastELISA)
- Dosage des contaminants Ig bovines (Kit RD-Biotech FastELISA)
Découvrir FastELISA - Dans le cadre de process High Quality Grade, des contrôles spécifiques seront appliqués
Nous consulter
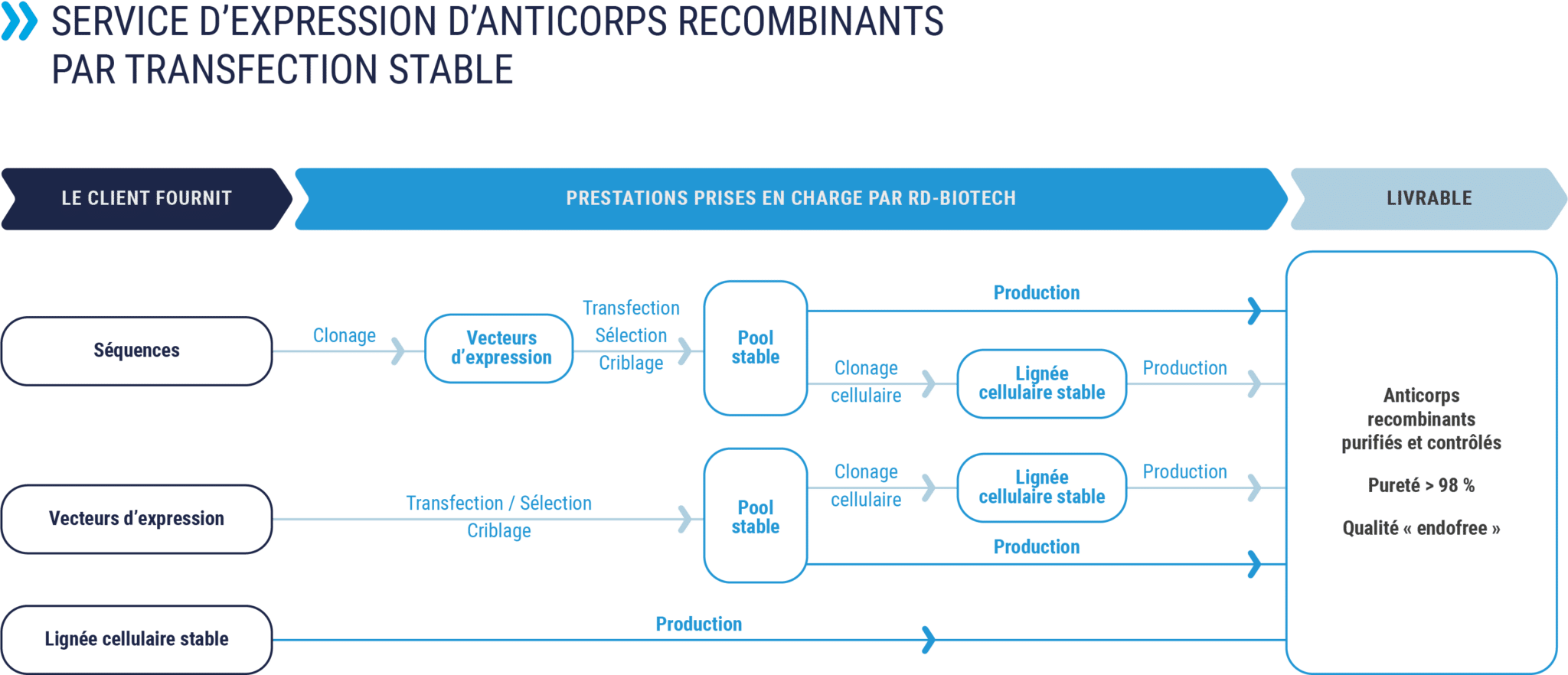
Production par transfection stable
Production des anticorps recombinants à partir d’une lignée cellulaire ou d’un pool de cellules stable, fourni par le donneur d’ordre ou développé par RD-Biotech.
Services à façon
Les anticorps recombinants présentent des avantages indéniables car ils sont produits selon un processus animal free, dans un environnement chimiquement et biologiquement défini, contrairement aux hybridomes.
RD-Biotech met au service de ses clients son expertise et son savoir-faire en ingénierie moléculaire & cellulaire pour modifier les anticorps recombinants et générer des variants selon vos cahiers des charges.
- Taux de succès > 98%
- Scale up Jusqu’à plusieurs centaines de mg
- Jusqu’à 50 variants
- Royalty-free
Les avantages :
- Pureté : pouvant atteindre des niveaux très élevés (> 98%) par l’expression en cellules mammifères et sans sérum, éliminant les risques de contamination par des composants sériques
- Diminution des délais de production
- Reproductibilité du process
- Ingénierie de l’anticorps
Séquençage de l'anticorps
RD-Biotech peut prendre en charge le séquençage des chaînes lourdes et légères de l’anticorps monoclonal candidat.
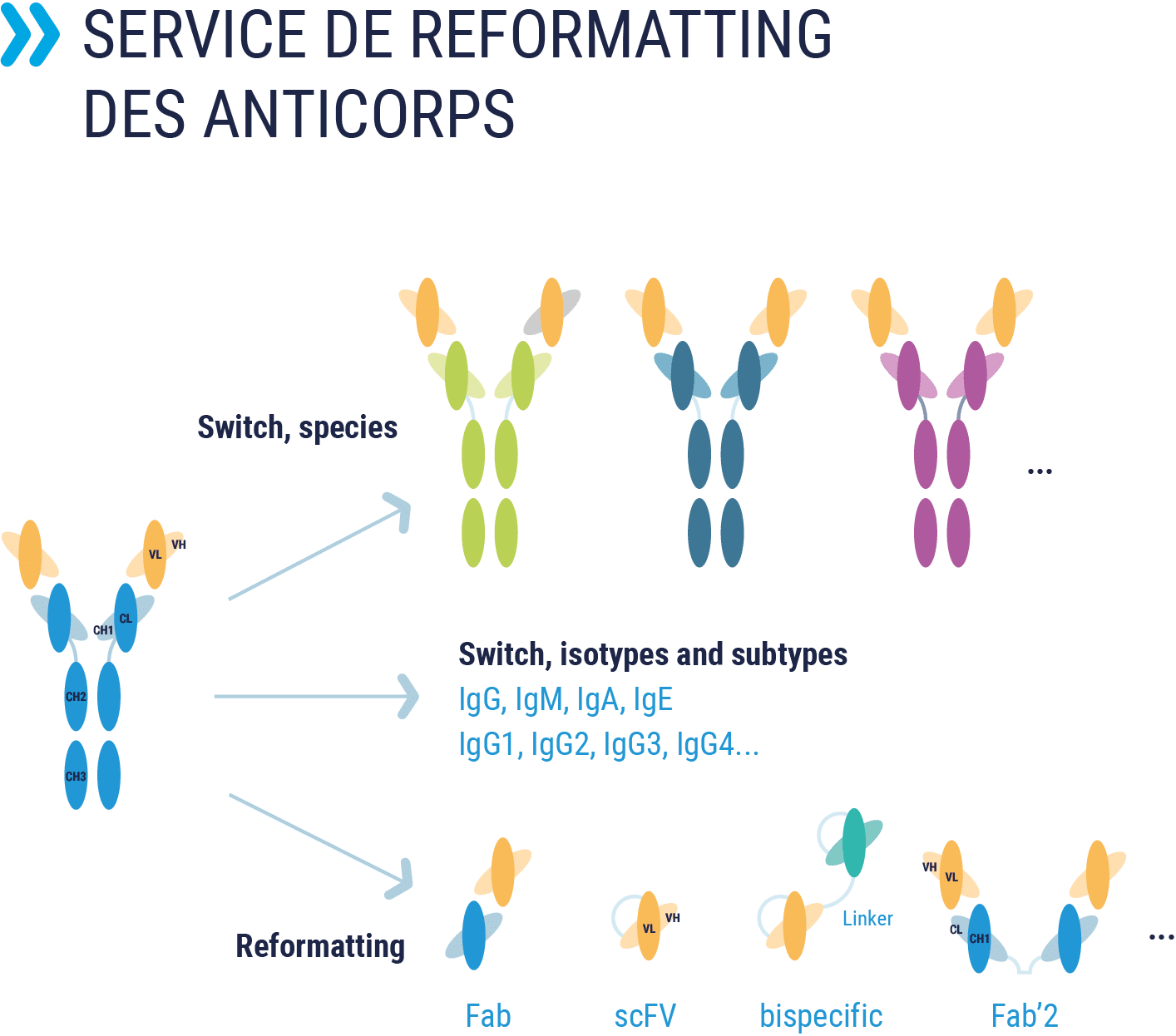
Reformatting d'anticorps
Service de reformatage de vos anticorps en de nombreux formats : scFv, fragments Fab, bispécifiques, changement d’isotypes ou de sous isotypes…
Chimérisation
Les anticorps chimériques sont constitués par l’association des régions variables d’un anticorps « parental » ou « donneur » avec les régions constantes d’un anticorps « accepteur » (d’une espèce différente). La combinaison des domaines variables murins et des domaines constants humains est la plus répandue mais d’autres combinaisons sont également réalisables.
La chimérisation constitue un processus simple et direct permettant de conserver l’affinité et la spécificité de l’anticorps parental.
- Développement de l’anticorps monoclonal parental (si demandé)
- Séquençage des fragments variables VH et VL de l’anticorps parental (si demandé)
- Construction des vecteurs d’expression : optimisation des codons, sélection des domaines constants (espèce et isotype), clonage des domaines variables VH et VL. Contrôles qualité.
Découvrir biologie moléculaire - Co-transfection et production des anticorps chimériques par transfection transitoire en cellules CHO
Découvrir anticorps recombinants - Evaluation de la productivité par ELISA (kits FastELISA)
Découvrir FastELISA - Purification par chromatographie d’affinité (résine protéine A, G, L…)
- Contrôles qualité (services analytiques)
- Contrôle de pureté par électrophorèse en gel SDS-PAGE (conditions réductrices et non réductrices)
- Dosage des protéines totales par mesure d’absorbance (spectrophotomètre)
- Contrôles supplémentaires proposés (en fonction du projet)
- SEC HPLCo Détermination de l’affinité
- Tests fonctionnels
- Autres tests disponibles
Humanisation
Les anticorps humanisés constituent la majorité des anticorps thérapeutiques approuvés sur le marché.
L’humanisation d’un anticorps parental (par exemple de souris) est réalisée suivant une version modernisée de “CDR-grafting” selon l’approche inventée par Winter et al. (« Medical Research Council » – Cambridge – UK). Le principe de cette méthode consiste à reformater un anticorps humain (séquences germinales) de manière à ce qu’il contienne les régions CDRs (Complementary Determinant Regions) de l’anticorps parental afin de réduire son immunogénicité chez l’homme. L’humanisation par “CDR-grafting” exige que les résidus de l’anticorps de souris impliqués dans la reconnaissance de l’antigène soient préservés dans la version humanisée de l’anticorps.
Suite à l’étape d’humanisation, une optimisation des séquences pourra être proposée avec en option des analyses complémentaires par modélisation moléculaire. L’objectif étant :
- L’augmentation de la manufacturabilité (réduction de l’hétérogénéité)
- L’augmentation possible de l’affinité et de l’activité biologique (IC50)
La procédure optimisée proposée par RD-Biotech comprend les étapes décrites ci-dessous :
Humanisation par CDR-grafting :
- Identification des régions charpentes (FRs) et des CDRs de l’anticorps parental
- Recherche et alignement des séquences de l’anticorps parental avec les séquences germinales humaines les plus homologues
- Identification des positions critiques
- Sélection d’une séquence germinale pour chaque chaîne (VH et VL) basée sur l’analyse de séquence et l’identification des positions critiques
- Evaluation de la pertinence de la substitution à chaque position divergente entre les séquences murine et humaine basée sur l’analyse structurale
- CDR-grafting par l’analyse des différences de séquence entre les séquences parentales et les séquences acceptatrices de l’anticorps
Optimisation des séquences :
- Amélioration de la manufacturabilité de l’anticorps et optimisation de son affinité et activité
- Fourniture d’un rapport intermédiaire comprenant la stratégie, les séquences aa des VL et VH de variants humanisés à synthétiser et à tester ainsi que les suggestions d’optimisation de séquences
Pour chaque construction, les étapes de construction des vecteurs d’expression, co-transfection, production et purification sont réalisées, selon les mêmes procédures que celles décrites dans le chapitre précédent « production par transfection transitoire ».
Les contrôles qualité comprennent :
- Contrôle de pureté par électrophorèse en gel SDS-PAGE (conditions réductrices et non réductrices)
- Dosage des protéines totales par mesure d’absorbance (spectrophotomètre)
- Contrôles supplémentaires proposés (en fonction du projet)
- SEC HPLC
- Détermination de l’affinité
- Tests fonctionnels (plateforme de bioessais)
- Autres tests disponibles, nous contacter
A l’issue de cette étape, un rapport est délivré, comprenant, pour chaque candidat, la stratégie suivie, les résultats obtenus et certificats d’analyses.
À partir d’un « lead candidat » identifié, un second cycle d’humanisation peut être proposé afin de substituer les éventuels résidus murins par leur homologues humains dans les régions « non CDR » et augmenter ainsi le % humain dans les VH et VL
- Optimisation de séquence afin d’éliminer les PTMs potentiels présents dans les CDRs
- Analyse complémentaire par modélisation
Ces différentes approches d’optimisation peuvent être menées en parallèle.
Caractérisation et validation des candidats
Spécificité, affinité, bioactivité, …
La plateforme analytique de RD-Biotech offre un large panel de services :
- Concentration, Pureté
- Détermination du taux d’endotoxines
- Détermination du taux d’agrégats
- Détermination du taux résiduel de contaminants : protéines A, ….
- Séquençage des parties variables VH et VL
- Analyse de la spécificité des anticorps recombinants : ELISA, Western Blot, …
- Analyse de l’affinité des anticorps recombinants : détermination des Kd, Kon, Koff grâce à la technologie Octet
- Analyse de stabilité : DSC
- Analyse de l’activité biologique des anticorps : large gamme de bio-essais (ADCC, ADCP, CDC, ….nous consulter) et service de développement à façon
Phage display
Grâce au savoir-faire de ses sociétés sœurs au sein de l’équipe mAbexperts, RD-Biotech propose le développement d’anticorps recombinants par la technologie de Phage Display :
Phage display chez la souris :
- Excellente alternative à la technologie hybridome
- Processus rapide (3 à 5 mois)
- Fourniture de banques naïves ou immunes (fab, scFv)
Phage display chez le lama :
Développement de vos VHH par immunisation de lamas et grâce à la technologie de phage display.
Autres services
Notre équipe commerciale ainsi que nos experts scientifiques et techniques sont à votre écoute pour vous proposer le service adapté à votre demande.